El peso atómico es una magnitud.
La fuerza desarrollada por el planeta para atraer a un cuerpo y la magnitud de dicha fuerza reciben el nombre de peso. El concepto también se emplea como sinónimo de masa (que, en realidad, es la cantidad de materia que alberga un cuerpo, independientemente de la fuerza de gravedad).
Atómico, por su parte, es un adjetivo que refiere a lo vinculado al átomo. Los átomos son las partículas indivisibles más pequeñas que disponen de existencia autónoma.
 Temas
TemasQué es el peso atómico
Estas definiciones nos ayudan a comprender la idea de peso atómico, una cantidad que revela el vínculo existente entre la masa de un átomo de una clase específica de isótopo y 1/12 de la masa de un átomo de carbono-12.
Esta magnitud, que también se conoce como masa atómica relativa, se expresa en unidades de masa atómica. Es importante diferenciar entre la masa atómica relativa o peso atómico y la masa atómica (que refiere a la masa de cada átomo individual).
Asignación de un número
Lo que permite el peso atómico es asignar un número a los elementos químicos para señalar cuál es la masa que tienen sus átomos en promedio. El peso atómico estará determinado de acuerdo a las proporciones de los isótopos, ya que un mismo elemento químico puede contar con más de un tipo de isótopo.
Se puede calcular un peso atómico a partir del valor conocido de la masa atómica y de acuerdo a la composición de los isótopos. El resultado de estas operaciones suele ser reflejado en la denominada tabla periódica de los elementos.
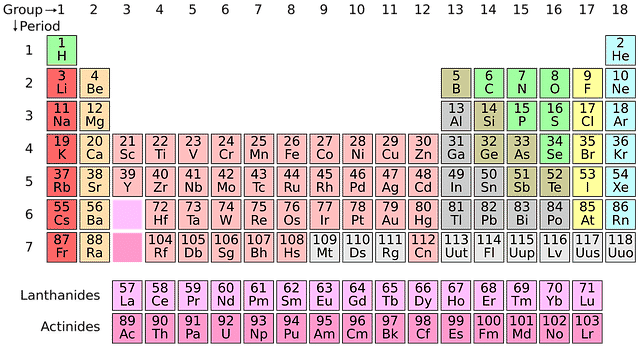
En la tabla periódica se suele indicar el peso atómico de los elementos.
Peso atómico, un concepto controvertido
Cabe mencionar que en el ámbito científico, la utilización del nombre «peso atómico» ha sido especialmente controvertida. Por lo general, los científicos prefieren referirse a este concepto como «masa atómica relativa» que, como se menciona anteriormente, no debe confundirse con la masa atómica. Para justificar dicha decisión, explican que esta propiedad no es un peso sino la fuerza que, en un campo gravitatorio, se ejerce sobre un objeto dado y que se mide en alguna unidad de fuerza, como puede ser el newton.
Por otro lado, aquellos científicos que están de acuerdo con referirse al concepto por el nombre de peso atómico señalan, entre otras cosas, que se trata de la denominación que ha recibido continuamente desde el año 1808, cuando el químico inglés John Dalton lo conceptualizó por primera vez. Dos siglos son demasiado tiempo como para erradicar su uso basándose simplemente en cuestiones semánticas, ya que se puede aceptar la imprecisión del nombre y no permitir que eso genere confusiones con respecto a lo que representa.
Puntos a favor de la noción
Otros puntos que apoyan el uso de peso atómico son los siguientes:
* si bien durante mucho tiempo el peso atómico se midió a través de la gravimetría (también denominada análisis gravimétrico), método que acarrea la acción de pesar, que esto haya cambiado no justifica la modificación del nombre originalmente asignado al concepto de esta cantidad física;
* el nombre «masa atómica relativa» debería quedar reservado para la masa de un isótopo (o nucleido específico);
* existen diversos ejemplos de nombres de cantidades físicas que no representan adecuadamente su significado, tal como ocurre con la potencia resolutiva, la concentración molar y la fuerza electromotriz, que no son fuerza ni potencia ni cantidad molar, respectivamente.
Peso atómico… que no es atómico
Por último, siendo verdaderamente meticulosos se puede alegar que el peso atómico no es realmente «atómico», ya que no hace referencia a un solo átomo. Claro que lo mismo puede argumentarse en detrimento del uso de «masa atómica relativa» cuando se refiere al mismo concepto.
Este fenómeno de nombres mal adjudicados también tiene lugar fuera de la ciencia y, del mismo modo, genera divisiones en el ámbito académico. Sin embargo, la denominación escogida de ninguna manera refleja la destreza de un científico, sino una preferencia personal que puede responder, por ejemplo, a una necesidad de ordenar los conceptos en su mente de una forma determinada.

